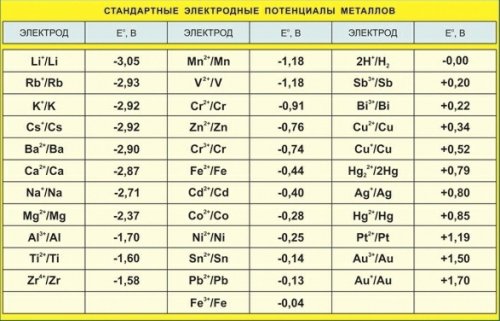
Tiềm năng của điện cực là gì
Thế điện cực hay thế điện cực của kim loại là hiệu điện thế xuất hiện ở mặt phân cách giữa kim loại và dung dịch khi kim loại được ngâm trong dung dịch điện phân do tương tác giữa các nguyên tử ion kim loại bề mặt nằm ở các nút của mạng tinh thể có cực. các phân tử nước hướng vào bề mặt của điện cực ... Điều này là do sự hình thành của một lớp điện kép, nghĩa là sự phân bố không đối xứng của các hạt tích điện ở ranh giới.
Hiện tượng hòa tan kim loại trong chất điện phân được sử dụng trong các nguồn điện hóa học. Một tấm kim loại được hun khói trong dung dịch muối của chính nó, bằng cách này hay cách khác, có xu hướng hòa tan trong đó. Xu hướng này đôi khi được gọi là độ đàn hồi hòa tan của kim loại.
Một tấm kẽm được ngâm trong dung dịch kẽm sulfat ZnTAKA4 cho các hạt kẽm vào dung dịch dưới dạng các ion tích điện dương.Do các nguyên tử màu hồng rời khỏi dạng ion tích điện dương, lượng electron tự do dư thừa được hình thành trên tấm kẽm và nó trở nên tích điện âm, và lượng ion dương dư thừa được hình thành trong lớp chất lỏng gần bề mặt của kẽm, và do đó lớp này được tải tích cực. Bằng cách này, một lớp điện kép gồm các điện tích trái dấu phân tách trong không gian phát sinh tại giao diện giữa chất lỏng và kim loại.
Các điện tích này sẽ chống lại sự di chuyển thêm của kim loại vào dung dịch—các bản cực âm giữ ion kim loại dương và điện tích dương của chất điện phân đẩy ion kim loại trở lại bản. Nói cách khác, điện trường của lớp kép ở giao diện kim loại-chất lỏng chống lại sự chuyển tiếp tiếp theo của các ion kim loại vào dung dịch. các lực điện trái dấu.
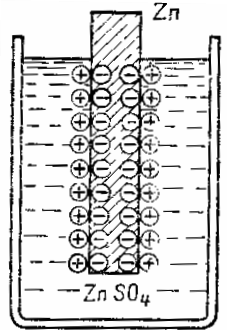
Sơ đồ tạo thành lớp kép điện ở mặt phân cách giữa kim loại và chất điện phân
Do đó, do hòa tan trong chất điện phân, điện cực kim loại thu được một điện thế nhất định (hay nói cách khác là điện hóa) đối với chất điện phân, điều này phụ thuộc vào vật liệu của điện cực và thành phần của chất điện phân.
Tuy nhiên, điện thế điện cực có thể dương. Điều này xảy ra trong trường hợp các ion dương của dung dịch đi đến điện cực, tích điện dương và lớp điện phân - tích điện âm, ví dụ, khi một tấm đồng được ngâm trong dung dịch đồng sunfat (CuSO)4 đủ đậm đặc).
Lớp kép điện có thể được ví như một tụ điện, một trong các bản tụ điện là bề mặt kim loại và bản kia là lớp ion trong dung dịch trên bề mặt kim loại. Giữa các bản tích điện trái dấu và có sự chênh lệch, hay còn gọi là bước nhảy, về điện thế.
Bước nhảy điện thế tại giao diện dung dịch điện cực có thể đóng vai trò là thước đo khả năng oxi hóa khử của hệ thống. Tuy nhiên, không thể đo được bước nhảy điện thế như vậy hay tương đương là hiệu điện thế giữa hai pha. Nhưng bạn có thể đo e. vân vân. c. các phần tử bao gồm các điện cực mà chúng ta quan tâm và một điện cực nào đó (giống nhau trong mọi trường hợp), điện thế của nó được giả định có điều kiện bằng không.
Nó đã được đo lường, vv c.sẽ đặc trưng cho khả năng oxi hóa khử của điện cực mà chúng ta quan tâm so với một số không có điều kiện. Giá trị do đó thu được được gọi là tiềm năng bên trong của kim loại.
Để đo thế điện cực của bất kỳ kim loại nào, cần đặt một điện cực thứ hai vào chất điện phân, do đó điện cực này sẽ có một thế điện cực nhất định, tùy thuộc vào vật liệu của nó. Do đó, chỉ có thể đo trực tiếp tổng đại số của hai thế điện cực.
Vì lý do này, thế điện cực của các vật liệu khác nhau được xác định đối với một tiêu chuẩn (điện cực hydro, thế của nó thường được coi là bằng không.
Các điện cực tham chiếu khác có điện thế so với điện cực chuẩn hydro đã biết cũng có thể được sử dụng để đo. Tiềm năng này cũng được tìm thấy dựa trên phép đo e. vân vân. c. một mạch bao gồm một điện cực tham chiếu đã chọn và một điện cực hydro tiêu chuẩn.
Nếu điện cực được nghiên cứu kết nối với điện cực hydro tiêu chuẩn là âm, thì dấu »-» được gán cho điện thế bên trong, nếu không, dấu «+».
Ví dụ, thế điện cực của kẽm -0,76 V, đồng +0,34 V, bạc +0,8 V, được đo theo cách này trong dung dịch muối kim loại tương ứng, được xác định bằng cách lấy điện thế dương trừ đi điện thế âm.
Nếu hai tấm kim loại có thế điện cực khác nhau được đặt trong chất điện phân tương ứng, ví dụ, trong dung dịch axit sunfuric (H2SO4) đặt kẽm (Zn) và đồng (Cth), thì vôn kế nối với các tấm này sẽ hiển thị hiệu điện thế giữa chúng hơn 1 V một chút.
Điện áp này, trong trường hợp này được gọi là e. vân vân. c. cặp galvanic, sẽ là do sự khác biệt về điện thế của đồng, có điện thế dương nhỏ và kẽm, có điện thế âm đáng kể. Một thiết bị như vậy là tế bào điện đơn giản nhất - tế bào Volta.
Trong một tế bào điện, năng lượng hóa học được chuyển đổi thành năng lượng điện và với sự trợ giúp của nó, có thể thực hiện công việc điện do năng lượng của phản ứng hóa học.
Phép đo của e. vân vân. c. Tế bào điện phải được tạo ra trong trường hợp không có dòng điện trong mạch tế bào. Mặt khác, e đo được. vân vân. s. sẽ nhỏ hơn giá trị được xác định là hiệu điện thế cân bằng của hai điện cực… Trên thực tế, một nồng độ nhất định của các electron trên các điện cực tương ứng với thế cân bằng: càng dương càng thấp, càng âm càng cao. Theo đó, cấu trúc của phần đó của lớp kép nằm trong dung dịch cũng khác nhau.
Phép đo của e. vân vân. vớimột tế bào không có dòng điện thường được tạo ra bằng phương pháp bù. Để áp dụng nó, bạn cần phải có một số tiêu chuẩn e.v.v. với Cái gọi là yếu tố bình thường phục vụ như một tiêu chuẩn như vậy. Thông thường nhất họ sử dụng nguyên tố thông thường thủy ngân-cadmium của Weston, ví dụ: vân vân. với.bằng 1,01830 V ở 20 ° C.